
Activité : propriétés de la matière
Un solide a une forme propre et on peut le saisir.
Un liquide adapte sa forme au récipient qui le contient.
La surface libre d'un liquide au repos est toujours horizontale.
Un gaz se disperse et occupe tout l’espace (le volume) qu’on lui offre.
La température de fusion/solidification de l'eau est de 0 °C (c'est une limite).
La température de vaporisation/liquéfaction de l'eau est de
100 °C.
soda bleue
lait bleue
huile blanc
glycérine blanc
vinaigre bleue
Tous les liquides ne contiennent pas d'eau.
à retenir :
- Le sulfate de cuivre anhydre est une poudre blanche qui sert à tester la présence d'eau.

Si le sulfate de cuivre devient bleu, alors le liquide à tester contient de l'eau.
Tableau de conversion :
kL |
hL |
daL |
L |
dL |
cL |
mL |
m3 |
|
|
dm3 |
|
|
cm3 |
Chapitre 2 : rendre une eau limpide
3) D'après le document 2, les deux derniers béchers nous donnent l'encadrement :
la masse de sel soluble se situe entre 15 g et 20 g.
C'est la masse soluble dans un volume de 50 mL d'eau.
4) Conversion :
1 L = 1 000 mL
50 x 20 = 1000 mL
Il y a donc 20 fois plus d'eau dans 1L que dans le bécher de 50 mL.
L'encadrement sera entre 300 g et 400 g.
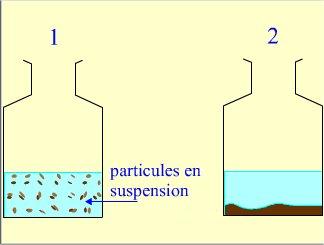
Les composants les plus denses tombent au fond du récipient.
à retenir :
Mélange homogène : mélange dans lequel on ne distingue pas les différents constituants.
Mélange hétérogène : mélange dans lequel on distingue les différents constituants.
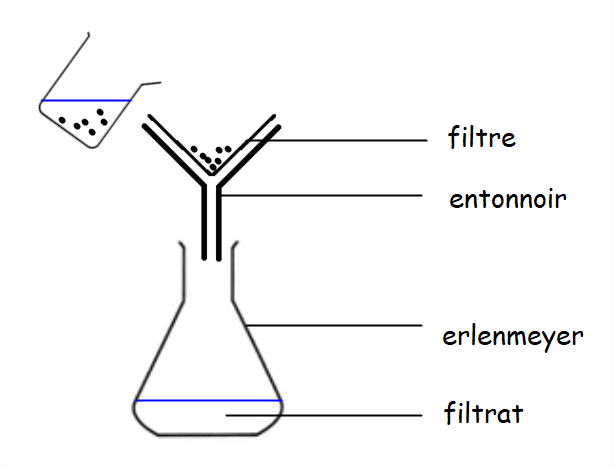
Savoir schématiser une filtration, une décantation.
Activité : distillation
Activité : comment définir la trajectoire d'un objet en mouvement ?
Page 185*